Порог удар нерв ожог
Нейропатическая боль
В статье описаны клинические подходы к диагностике нейропатической боли, приведены Британские рекомендации по лечению нейропатической боли в общесоматической практике и возможности повышения эффективности терапии, в частности рациональное использование комплекса витаминов В в комбинации с габапептиноидами.
Причиной центральной нейропатической боли может являться инсульт, спинальная травма, рассеянный склероз. Нейропатические боли часто ассоциированны с сахарным диабетом, хроническим приемом алкоголя, дефицитом витаминов, хронической болью в спине, радикулярной болью, онкологическими заболеваниями.
Но зачастую конкретная причина нейропатической боли может быть не установлена даже после обследования в специализированном центре.
Поэтому нейропатическая боль может быть разделена на две категории: 1) Хроническое болевое расстройство с нейропатическими характеристиками. 2) Нейропатическая боль, связанная с определенным состоянием.
Нейропатическая боль — это особо тяжёлый вариант хронической боли, проявляющийся интенсивными жгучими или простреливающими болями, продолжающимися в течение длительного времени, до нескольких месяцев. Боль может усиливаться ночью в покое. Пациенты описывают боль как, как жжет, горит, ноет, скребет, дергает, бьет током.
Эти боли возникать спонтанно, т. е. не связанно с обычными провоцирующими факторами (движение, прикосновение к болевой зоне), болевых или других неприятных ощущений (дизестезия). Боль может сопровождается набором чувствительных расстройств, таких как парестезии (покалывание, ползание мурашек), гипералгезия (избыточный ответ на обычный болевой стимул) и аллодиния. Аллодиния — это когда пациент испытывает болевые ощущения в ответ на неболевые раздражения, когда простое легкое прикосновение, холод или тепло приводят к появлению или усилению боли. Аллодиния может быть настолько выражена, что даже прикосновение одежды является очень мучительным для пациента. Даже малейшего ветерка достаточно, чтобы вызвать боль.
У пациентов в зоне болевых ощущений или рядом могут располагаться участки пониженной чувствительности (гипостезия). Эти симптомы свидетельствуют о повреждении и/или гибели отдельных нервных волокон. Гипостезия является частым, но не обязательным симптомом нейропатической боли. При осмотре в зоне болевых ощущений можно выявить трофические изменения: истончение кожи, подкожной клетчатки, нарушение роста волос, ногтей, сухость кожных покровов, изменения дермографизма, цвета и температуры кожи, что свидетельствует о вовлечении в процесс вегетативных волокон.
Боль всегда сопровождается негативными эмоциями. Психопатологические последствия нейропатической боли включают симптомы нарушения настроения, тревоги [2]. Распространенность депрессивных и тревожных расстройств у пациентов с нейропатической болью как минимум в два раза превосходит этот показатель в общей популяции.
Боль вызывает негативные эмоции, которые приводят к изменению порога болевой чувствительности. Это в свою очередь ведет к персистированию болевых симптомов. Депрессия и тревога воздействуют на механизмы формирования и поддержания боли, являются важными модуляторами боли, усиливают интенсивность боли, увеличивают поверхность распространения болевых ощущений. И, наконец, депрессия является независимым фактором нарушения трудоспособности и социальной адаптации у лиц, страдающих хроническим болевым расстройством. У пациентов с нейропатической болью и депрессией качество жизни ниже, а интенсивность боли выше. Около 50%-80% пациентов, страдающих нейропатической болью, имеют нарушения сна с дневными последствиями: усталость, сонливость, нарушение концентрации внимания. Снижается общая эффективность сна. Бессонница также может быть дополнительным фактором риска для развития депрессии и других психопатологических состояний. Таким образом, нейропатическая боль сопряжена с инсомнией и тревожно-депрессивными расстройствами, которые утяжеляют картину боли.
Ученые признают базисные универсальные механизмы, лежащие в основе нейропатической боли, независимо от природы повреждения. Поврежденные нервные волокна претерпевают функциональные изменения, вследствие чего непрерывно посылают неправильные сигналы в другие болевые центры. Изменения, обусловливающие развитие нейрогенного болевого синдрома, происходят как на периферическом уровне, так и в ЦНС.
Лечение нейропатической боли
В начале терапии болевого синдрома, сначала по возможности возможности следует устраненить этиологический фактор. Однако лечение основного заболевания и даже его полное купирование не всегда приводят к исчезновению болевого синдрома. Поэтому собственно боль рассматривается врачом как целевая мишень для терапии, не зависящая от природы повреждения. Перед началом терапии проводится разъяснительная беседа с больным и его родственниками суть которой заключается в том, что лечение может быть длительным, и уменьшение боли будет происходить постепенно. Даже при правильной программе лечения редко удается достичь полного обезболивания. Хорошим результатом считается снижение интенсивности боли на 30%-50% от исходного уровня. Этот параметр следует иметь в виду при оценке эффективности проводимого лечения и решении вопросов о переходе на другой препарат или присоединении нового лекарства к уже принимаемому препарату.
Британские рекомендации по лечению нейропатической боли в общеврачебной практике 2013 г, модернизированные в 2017 г., предлагают в качестве начальной терапии для нейропатической боли любого происхождения, за исключением тригеминальной невралгии, выбор из следующих препаратов: амитриптилин, дулоксетин, габапентин или прегабалин [9]. Из перечисленных препаратов наилучшей переносимостью обладают габапептиноиды (прегабалин, габапентин). Эти препараты характеризуются практически полным отсутствием лекарственных взаимодействий и сравнительно невысокой частотой развития нежелательных явлений. Пациентом с локализованной нейропатической болью на начальном этапе лечения альтернативно можно рекомендовать средства для наружного применения, содержащие капсаицин. Если первоначальное лечение не является эффективным или плохо переносится пациентом, нужно перевести пациента на альтернативную монотерапию препаратом первого ряда или предложить пациенту комбинацию из двух препаратов разных классов. Неэффективное первоначальное лечение требует консультации со специалистом (невролог, альголог) для обсуждения вопроса о назначении препаратов второй линии (лакосамид, ламотриджин, леветирацетам, окскарбазепин, топирамат, венлафаксин, трамадол).
Комбинированная терапия обычно считаются более эффективной, чем монотерапия, но неясно, какие комбинации лучше. Очень мало рандомизированных исследований, посвященных комбинированной терапии нейропатической боли. Но по факту комбинированная терапия используется чрезвычайно широко. К самым часто используемым дополнительным средствам относят Acetyl-L-carnitine, витамины группы В, альфа-липоевая кислота, магнезия [10]. Витамины B1, B6 и B12 действуют в основном как коферменты различных реакций, участвуя в метаболизме углеводов, белков и липидов. Они также играют важную роль в формировании новых клеток, ДНК, РНК и миелина. Абсолютным показанием для их назначения являются состояния, вызванные дефицитом этих витаминов. Дефицит витамина B12 часто наблюдается у пациентов, принимающих метформин, что требует назначения витамина B12 в ежедневной дозе 1000 мкг. Бенфотиамин (жирорастворимая форма тиамина- вит. В1) считается наилучшим вариантом, потому что он лучше проникает через мембраны клетки.
Учет международного и Российского опыта позволяет рекомендовать в качестве инициальной терапии нейропатической боли габапентин (Габагамма) в комбинации с нейротропной терапией Мильгамма в/м №10, с последующим переходом на Мильгамму композитум по 1 драже 3 раза в день шесть недель. Целевая доза габапентина составляет 900 мг/сут., разделенная на 3 приема. При необходимости через 2-4 недели дозу увеличивают.
Лечение нейропатической боли на сегодняшний день продолжает оставаться сложной задачей. Представленные выше принципы и схемы лечения помогают врачу проводить наиболее эффективное и безопасное лечение пациентов с нейропатическим болевым синдромом. Однако, при недостаточной эффективности первоначальной терапии, они не могут заменить индивидуальные консультации со специалистами в конкретных случаях.
Причиной центральной нейропатической боли может являться инсульт, спинальная травма, рассеянный склероз. Нейропатические боли часто ассоциированны с сахарным диабетом, хроническим приемом алкоголя, дефицитом витаминов, хронической болью в спине, радикулярной болью, онкологическими заболеваниями.
Но зачастую конкретная причина нейропатической боли может быть не установлена даже после обследования в специализированном центре.
Поэтому нейропатическая боль может быть разделена на две категории: 1) Хроническое болевое расстройство с нейропатическими характеристиками. 2) Нейропатическая боль, связанная с определенным состоянием.
Нейропатическая боль — это особо тяжёлый вариант хронической боли, проявляющийся интенсивными жгучими или простреливающими болями, продолжающимися в течение длительного времени, до нескольких месяцев. Боль может усиливаться ночью в покое. Пациенты описывают боль как, как жжет, горит, ноет, скребет, дергает, бьет током.
Эти боли возникать спонтанно, т. е. не связанно с обычными провоцирующими факторами (движение, прикосновение к болевой зоне), болевых или других неприятных ощущений (дизестезия). Боль может сопровождается набором чувствительных расстройств, таких как парестезии (покалывание, ползание мурашек), гипералгезия (избыточный ответ на обычный болевой стимул) и аллодиния. Аллодиния — это когда пациент испытывает болевые ощущения в ответ на неболевые раздражения, когда простое легкое прикосновение, холод или тепло приводят к появлению или усилению боли. Аллодиния может быть настолько выражена, что даже прикосновение одежды является очень мучительным для пациента. Даже малейшего ветерка достаточно, чтобы вызвать боль.
У пациентов в зоне болевых ощущений или рядом могут располагаться участки пониженной чувствительности (гипостезия). Эти симптомы свидетельствуют о повреждении и/или гибели отдельных нервных волокон. Гипостезия является частым, но не обязательным симптомом нейропатической боли. При осмотре в зоне болевых ощущений можно выявить трофические изменения: истончение кожи, подкожной клетчатки, нарушение роста волос, ногтей, сухость кожных покровов, изменения дермографизма, цвета и температуры кожи, что свидетельствует о вовлечении в процесс вегетативных волокон.
Боль всегда сопровождается негативными эмоциями. Психопатологические последствия нейропатической боли включают симптомы нарушения настроения, тревоги [2]. Распространенность депрессивных и тревожных расстройств у пациентов с нейропатической болью как минимум в два раза превосходит этот показатель в общей популяции.
Боль вызывает негативные эмоции, которые приводят к изменению порога болевой чувствительности. Это в свою очередь ведет к персистированию болевых симптомов. Депрессия и тревога воздействуют на механизмы формирования и поддержания боли, являются важными модуляторами боли, усиливают интенсивность боли, увеличивают поверхность распространения болевых ощущений. И, наконец, депрессия является независимым фактором нарушения трудоспособности и социальной адаптации у лиц, страдающих хроническим болевым расстройством. У пациентов с нейропатической болью и депрессией качество жизни ниже, а интенсивность боли выше. Около 50%-80% пациентов, страдающих нейропатической болью, имеют нарушения сна с дневными последствиями: усталость, сонливость, нарушение концентрации внимания. Снижается общая эффективность сна. Бессонница также может быть дополнительным фактором риска для развития депрессии и других психопатологических состояний. Таким образом, нейропатическая боль сопряжена с инсомнией и тревожно-депрессивными расстройствами, которые утяжеляют картину боли.
Ученые признают базисные универсальные механизмы, лежащие в основе нейропатической боли, независимо от природы повреждения. Поврежденные нервные волокна претерпевают функциональные изменения, вследствие чего непрерывно посылают неправильные сигналы в другие болевые центры. Изменения, обусловливающие развитие нейрогенного болевого синдрома, происходят как на периферическом уровне, так и в ЦНС.
Лечение нейропатической боли
В начале терапии болевого синдрома, сначала по возможности возможности следует устраненить этиологический фактор. Однако лечение основного заболевания и даже его полное купирование не всегда приводят к исчезновению болевого синдрома. Поэтому собственно боль рассматривается врачом как целевая мишень для терапии, не зависящая от природы повреждения. Перед началом терапии проводится разъяснительная беседа с больным и его родственниками суть которой заключается в том, что лечение может быть длительным, и уменьшение боли будет происходить постепенно. Даже при правильной программе лечения редко удается достичь полного обезболивания. Хорошим результатом считается снижение интенсивности боли на 30%-50% от исходного уровня. Этот параметр следует иметь в виду при оценке эффективности проводимого лечения и решении вопросов о переходе на другой препарат или присоединении нового лекарства к уже принимаемому препарату.
Британские рекомендации по лечению нейропатической боли в общеврачебной практике 2013 г, модернизированные в 2017 г., предлагают в качестве начальной терапии для нейропатической боли любого происхождения, за исключением тригеминальной невралгии, выбор из следующих препаратов: амитриптилин, дулоксетин, габапентин или прегабалин [9]. Из перечисленных препаратов наилучшей переносимостью обладают габапептиноиды (прегабалин, габапентин). Эти препараты характеризуются практически полным отсутствием лекарственных взаимодействий и сравнительно невысокой частотой развития нежелательных явлений. Пациентом с локализованной нейропатической болью на начальном этапе лечения альтернативно можно рекомендовать средства для наружного применения, содержащие капсаицин. Если первоначальное лечение не является эффективным или плохо переносится пациентом, нужно перевести пациента на альтернативную монотерапию препаратом первого ряда или предложить пациенту комбинацию из двух препаратов разных классов. Неэффективное первоначальное лечение требует консультации со специалистом (невролог, альголог) для обсуждения вопроса о назначении препаратов второй линии (лакосамид, ламотриджин, леветирацетам, окскарбазепин, топирамат, венлафаксин, трамадол).
Комбинированная терапия обычно считаются более эффективной, чем монотерапия, но неясно, какие комбинации лучше. Очень мало рандомизированных исследований, посвященных комбинированной терапии нейропатической боли. Но по факту комбинированная терапия используется чрезвычайно широко. К самым часто используемым дополнительным средствам относят Acetyl-L-carnitine, витамины группы В, альфа-липоевая кислота, магнезия [10]. Витамины B1, B6 и B12 действуют в основном как коферменты различных реакций, участвуя в метаболизме углеводов, белков и липидов. Они также играют важную роль в формировании новых клеток, ДНК, РНК и миелина. Абсолютным показанием для их назначения являются состояния, вызванные дефицитом этих витаминов. Дефицит витамина B12 часто наблюдается у пациентов, принимающих метформин, что требует назначения витамина B12 в ежедневной дозе 1000 мкг. Бенфотиамин (жирорастворимая форма тиамина- вит. В1) считается наилучшим вариантом, потому что он лучше проникает через мембраны клетки.
Учет международного и Российского опыта позволяет рекомендовать в качестве инициальной терапии нейропатической боли габапентин (Габагамма) в комбинации с нейротропной терапией Мильгамма в/м №10, с последующим переходом на Мильгамму композитум по 1 драже 3 раза в день шесть недель. Целевая доза габапентина составляет 900 мг/сут., разделенная на 3 приема. При необходимости через 2-4 недели дозу увеличивают.
Лечение нейропатической боли на сегодняшний день продолжает оставаться сложной задачей. Представленные выше принципы и схемы лечения помогают врачу проводить наиболее эффективное и безопасное лечение пациентов с нейропатическим болевым синдромом. Однако, при недостаточной эффективности первоначальной терапии, они не могут заменить индивидуальные консультации со специалистами в конкретных случаях.
Статья добавлена 3 июля 2019 г.
Источник
Повреждение нерва
Повреждение нерва — это полное или частичное нарушение целостности нерва вследствие ранения, удара или сдавления. Может возникать при любых видах травм. Сопровождается нарушением чувствительности, выпадением двигательных функций и развитием трофических расстройств в зоне иннервации. Является тяжелым повреждением, нередко становится причиной частичной или полной нетрудоспособности. Диагноз устанавливают на основании клинических признаков и данных стимуляционной электромиографии. Лечение комплексное, сочетает консервативные и оперативные мероприятия.
Общие сведения
Повреждение нерва — распространенная тяжелая травма, обусловленная полным или частичным перерывом нервного ствола. Нервная ткань плохо регенерирует. К тому же, при подобных травмах в дистальной части нерва развивается Валлерова дегенерация — процесс, при котором нервная ткань рассасывается и замещается рубцовой соединительной тканью. Поэтому благоприятный исход лечения трудно гарантировать даже при высокой квалификации хирурга и адекватном восстановлении целостности нервного ствола. Повреждения нервов часто становятся причиной ограничения трудоспособности и выхода на инвалидность. Лечение таких травм и их последствий осуществляют врачи-нейрохирурги и травматологи.
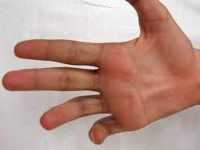
Повреждение нерва
Причины
Закрытые повреждения нерва возникают вследствие сдавления мягких тканей посторонним предметом (например, при нахождении под завалом), удара тупым предметом, изолированного сдавления нерва опухолью, отломком кости при переломе или вывихнутым концом кости при вывихе. Открытые повреждения нерва в мирное время чаще становятся следствием резаных ран, в период военных действий — огнестрельных ранений. Закрытые повреждения, как правило, бывают неполными, поэтому протекают более благоприятно.
Патогенез
Повреждения нерва сопровождаются выпадением чувствительности, нарушением двигательной функции и трофическими расстройствами. В автономной зоне иннервации чувствительность полностью отсутствует, в смешанных зонах (областях перехода иннервации от одного нерва к другому) выявляются участки снижения чувствительности, перемежающиеся участками гиперпатии (извращения чувствительности, при котором в ответ на действие безвредных раздражителей возникает боль, зуд или другие неприятные ощущения). Нарушение двигательных функций проявляется вялым параличом иннервируемых мышц.
Кроме того, в области поражения развивается ангидроз кожи и вазомоторные нарушения. В течение первых трех недель наблюдается горячая фаза (кожа красная, ее температура повышена), которая сменяется холодной фазой (кожа становится холодной и приобретает синюшный оттенок). Со временем в пораженной области возникают трофические расстройства, характеризующиеся истончением кожи, снижением ее тургора и эластичности. В отдаленные сроки выявляется тугоподвижность суставов и остеопороз.
Классификация
В зависимости от тяжести повреждения нерва в практической неврологии и травматологии выделяют следующие расстройства:
- Сотрясение. Морфологические и анатомические нарушения отсутствуют. Чувствительность и двигательные функции восстанавливаются через 10-15 сут. после травмы.
- Ушиб (контузия). Анатомическая непрерывность нервного ствола сохранена, возможны отдельные повреждения эпиневральной оболочки и кровоизлияния в ткань нерва. Функции восстанавливаются примерно через месяц после повреждения.
- Сдавление. Выраженность расстройств напрямую зависит от тяжести и длительности сдавления, могут наблюдаться как незначительные преходящие нарушения, так и стойкое выпадение функций, требующее проведения оперативного вмешательства.
- Частичное повреждение. Отмечается выпадение отдельных функций, нередко — в сочетании с явлениями раздражения. Самопроизвольного восстановления, как правило, не происходит, необходима операция.
- Полный перерыв. Нерв разделяется на два конца — периферический и центральный. При отсутствии лечения (а в ряде случаев и при адекватном лечении) срединный фрагмент замещается участком рубцовой ткани. Самопроизвольное восстановление невозможно, в последующем наблюдается нарастающая атрофия мышц, нарушения чувствительности и трофические расстройства. Требуется хирургическое лечение, однако, результат не всегда бывает удовлетворительным.
Симптомы повреждения нерва
Повреждение локтевого нерва, в первую очередь проявляется двигательными расстройствами. Активное сгибание, разведение и сведение V и IV и частично III пальцев невозможно, сила мышц резко ослаблена. В течение 1-2 месяцев развивается атрофия межкостных мышц, вследствие чего на тыле кисти начинают резко выделяться контуры пястных костей. В отдаленном периоде возникает характерная деформация кисти в форме когтя. Средние и дистальные фаланги V и IV пальцев находятся в состоянии сгибания. Противопоставление мизинца невозможно. По локтевой стороне кисти наблюдаются расстройства чувствительности, секреторные и вазомоторные нарушения.
Повреждение срединного нерва сопровождается выраженным нарушением чувствительности. Кроме того, уже в начальном периоде хорошо заметны трофические, секреторные и вазомоторные нарушения. Кожа иннервируемой области шелушащаяся, блестящая, цианотичная, сухая, гладкая и легкоранимая. Ногти I-III пальцев поперечно исчерчены, подкожная клетчатка ногтевых фаланг атрофирована. Характер двигательных расстройств определяется уровнем повреждения нерва.
Низкие поражения сопровождаются параличом мышц тенара, высокие — нарушением ладонного сгибания кисти, пронации предплечья, разгибания средних фаланг III и II пальца, сгибания I-III пальцев. Противопоставление и отведение I пальца невозможно. Мышцы постепенно атрофируются, развивается их фиброзная дегенерация, поэтому при давности травмы свыше года восстановление их функции становится невозможным. Формируется «обезьянья кисть».
Повреждение лучевого нерва на уровне плеча или подмышечной области сопровождается яркими двигательными нарушениями. Возникает паралич разгибателей кисти и предплечья, проявляющийся симптомом свисающей или «падающей» кисти. При повреждении нижележащих отделов развиваются только расстройства чувствительности (обычно по типу гипестезии). Страдает тыльная поверхность лучевой стороны кисти и фаланг I-III пальцев.
Повреждение седалищного нерва проявляется нарушением сгибания голени, параличом пальцев и стопы, потерей чувствительности по задней поверхности бедра и практически по всей голени (за исключением внутренней поверхности), а также утратой ахиллова рефлекса. Возможна каузалгия — мучительные жгучие боли в зоне иннервации травмированного нерва, распространяющиеся на всю конечность, а иногда и на туловище. Часто наблюдается частичное повреждение нерва с выпадением функций его отдельных ветвей.
Повреждение большеберцового нерва проявляется выпадением ахиллова рефлекса, нарушением чувствительности наружного края стопы, подошвы и задней поверхности голени. Формируется типичная деформация: стопа разогнута, задняя группа мышц голени атрофирована, пальцы согнуты, свод стопы углублен, пятка выступает. Ходьба на носках, поворот стопы кнутри, а также сгибание пальцев и стопы невозможны. Как и в предыдущем случае, нередко развивается каузалгия.
Повреждение малоберцового нерва сопровождается параличом разгибателей пальцев и стопы, а также мышц, которые обеспечивают поворот стопы кнаружи. Отмечаются нарушения чувствительности по тылу стопы и наружной поверхности голени. Формируется характерная походка: пациент высоко поднимает голень, сильно сгибая колено, затем опускает ногу на носок и только потом на подошву. Каузалгия и трофические расстройства, как правило, не выражены, ахиллов рефлекс сохранен.
Диагностика
В постановке диагноза важнейшую роль играют осмотр, пальпация и неврологическое исследование. При осмотре обращают внимание на типичные деформации конечности, цвет кожи, трофические нарушения, вазомоторные расстройства и состояние различных групп мышц. Все данные сравнивают со здоровой конечностью. При пальпации оценивают влажность, эластичность, тургор и температуру различных участков конечности. Затем проводят исследование чувствительности, сравнивая ощущения в здоровой и больной конечности. Определяют тактильную, болевую и температурную чувствительность, чувство локализации раздражения, суставно-мышечное чувство, стереогнозис (узнавание предмета на ощупь, без контроля зрения), а также чувство двухмерных раздражений (определение фигур, цифр или букв, которые врач «рисует» на коже пациента).
Ведущим дополнительным методом исследования в настоящее время является стимуляционная электромиография. Эта методика позволяет оценить глубину и степень повреждения нерва, выяснить скорость проведения импульсов, функциональное состояние рефлекторной дуги и т. д. Наряду с диагностической ценностью, данный метод имеет и определенное прогностическое значение, поскольку позволяет выявлять ранние признаки восстановления нерва.
Лечение повреждения нерва
Лечение комплексное, используются как хирургические методики, так и консервативная терапия. Консервативные мероприятия начинают с первых дней после травмы или оперативного вмешательства и продолжают вплоть до полного выздоровления. Их цель — предупреждение развития контрактур и деформаций, стимуляция репаративных процессов, улучшение трофики, поддержание тонуса мышц, профилактика фиброза и рубцевания. Применяют ЛФК, массаж и физиолечение, в том числе — УВЧ, электрофорез с новокаином, кальцием и гиалуронидазой, парафин, озокерит и электростимуляцию. Назначают медикаментозно-стимулирующую терапию: витамины В12 и В1, бендазол с никотиновой кислотой, АТФ.
Показаниями к операции являются вегетативно-трофические расстройства, нарушения чувствительности и двигательные расстройства в зоне иннервации поврежденного нерва. В зависимости от характера травмы и рубцовых изменений может быть проведен невролиз (иссечение рубцов оболочки нерва), эпиневральный шов (сопоставление нерва и сшивание его оболочки) или пластика нерва. При этом широко применяются микрохирургические техники, позволяющие точно сопоставлять идентичные пучки поврежденных концов нервного ствола.
Прогноз и профилактика
Наилучшие результаты достигаются при ранних хирургических вмешательствах — в среднем не более 3 месяцев с момента травмы, при травмах нервов кисти — не более 3-6 месяцев с момента травмы. Если операция по каким-то причинам не была проведена в ранние сроки, ее следует выполнить в отдаленном периоде, так как восстановительные хирургические мероприятия практически всегда позволяют в той или иной степени улучшить функцию конечности. Однако на существенное улучшение двигательных функций при поздних вмешательствах рассчитывать не стоит, поскольку мышцы с течением времени подвергаются фиброзному перерождению. Профилактика включает меры по предупреждению травм, своевременное лечение заболеваний, которые могут стать причиной повреждения нерва.
Источник